CEI-SoHO
Comité de Evaluación de la Innovación en Sustancias de Origen Humano (CEi-SoHO)
En los últimos años se ha intensificado el uso de sustancias de origen humano (SoHO) para nuevas aplicaciones y usos innovadores dentro del ámbito de los trasplantes, en algunos casos gracias al desarrollo de tecnologías que permiten su procesamiento inmediato dentro del quirófano o incluso de forma ambulatoria. También estamos asistiendo a la creciente actividad de desarrollo, investigación y uso clínico de productos derivados de SoHO regulados como productos sanitarios o medicamentos de terapia avanzada (TA) que, para su fabricación requieren células y tejidos humanos ya donados o no donados aún, tanto autólogos como alogénicos, cuya donación se regula por el nuevo Reglamento, de plena aplicación el 7 de agosto de 2027, derogando las directivas anteriores en esta materia.
Hematopoyéticos (TPH), dependientes de la Comisión Permanente de Trasplantes del Consejo Interterritorial (CIT) del Sistema Nacional de Salud (SNS) en el desempeño de aquellas funciones que pudieran solaparse.
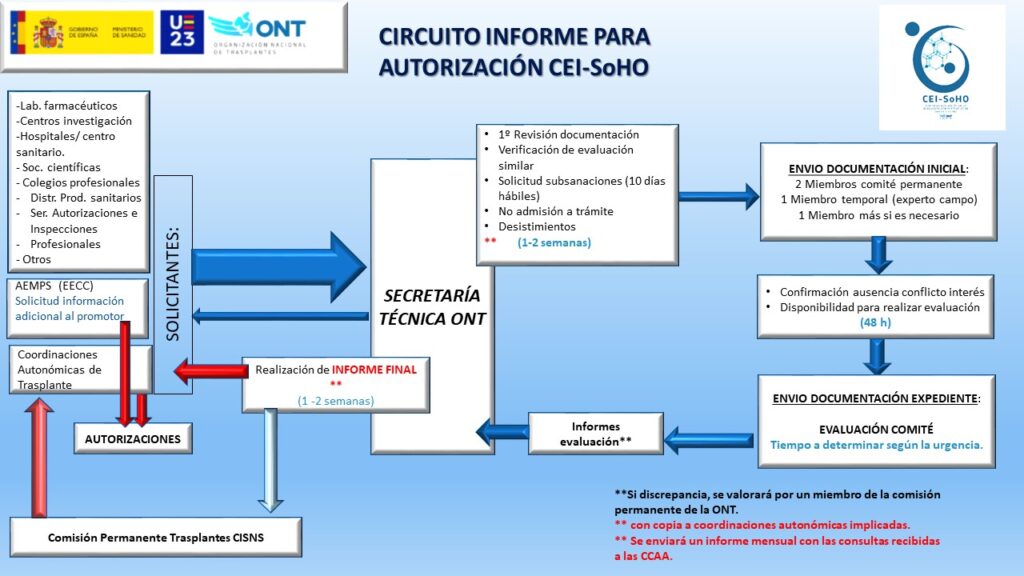
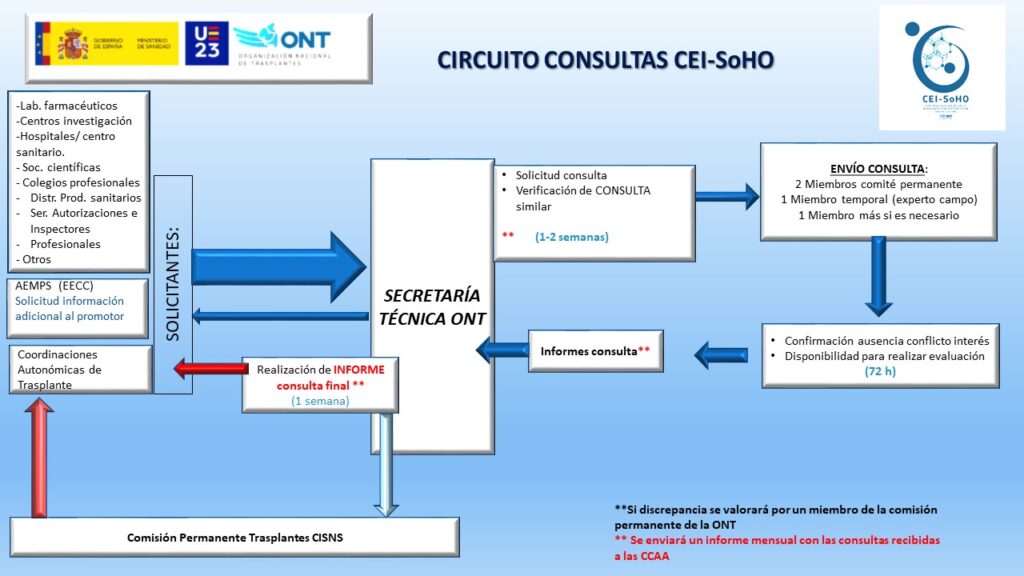
Procesos actuales
Guías y documentos
- Cómo solicitar una evaluación:
- Cómo solicitar la autorización de preparados:
- Infografía: Solicitud Proceso de Preparación
- ANEXO III. Solicitud autorización preparados.
- Infografía: Evaluación de Riesgo
- Solicitud de autorización excepcional (en elaboración)
Correo de contacto: innovacion.ont@sanidad.gob.es
- Actualizado el 26 de marzo de 2026